Остановка по требованию
Разработка новосибирских учёных в перспективе может увеличить количество трансплантаций сердца на 20–30 процентов

Хирурги восстанавливают работу сердца после 20-минутной остановки.
В национальном медицинском исследовательском центре имени академика Мешалкина группа молодых учёных проводит серию экспериментов по восстановлению и реабилитации донорских сердец после остановки кровообращения. Сейчас такие органы считаются непригодными для трансплантации.
Речь идёт об остановившихся сердцах доноров — пациентов с диагностированной смертью головного мозга. Учёные выясняют, можно ли их использовать для трансплантации, если был перерыв в кровообращении, и каким по длительности может быть такой перерыв.
В группу под руководством старшего научного сотрудника кандидата медицинских наук Максима Жулькова входят аспиранты Андрей Протопопов и Александр Макаев, которые в 2025 году стали получателями стипендий правительства области. Сердечно-сосудистые хирурги провели уже более десятка экспериментов на крупных лабораторных животных. Журналистам продемонстрировали один из них.
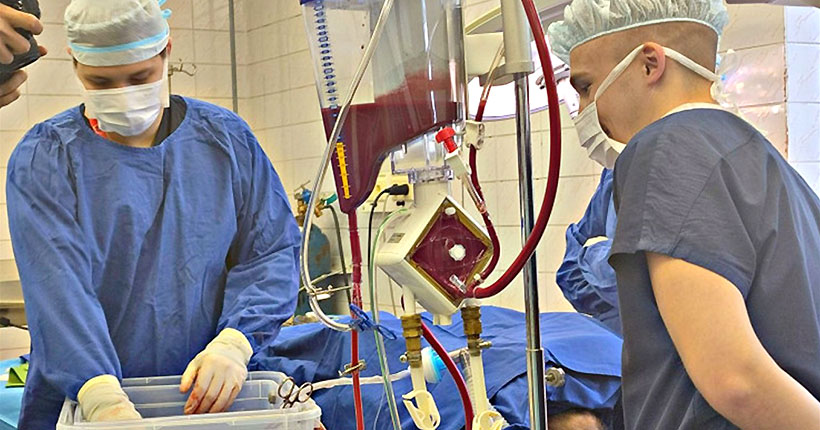
В ходе операции с помощью аппарата искусственного кровообращения из тела забирается венозная кровь, наступает остановка кровообращения, сердце сокращается всё реже и реже, затем переходит в фибрилляцию и, наконец, останавливается. На мониторе, где во время операции отражаются все параметры, хаотично колеблющуюся линию сердечных сокращений сменяет ровная прямая. Начинается отсчёт перерыва в работе сердца — в эксперименте он составляет 20 минут. По истечении этого времени аппарат начинает подавать в тело кровь, обеспечивается её циркуляция, постепенно восстанавливаются желудочки сердца. На мониторе прямая линия вновь оживает, начинает подёргиваться — это хаотичное некоординируемое движение отдельных участков миокарда. Ещё через несколько минут врач производит дефибрилляцию — разряд тока должен помочь восстановить ритм сердца. И действительно — на экране появляются ровные пики, как на привычной кардиограмме. Отключается аппарат искусственного кровообращения — сердце уверенно качает кровь самостоятельно.
— Вторая часть работы, которую мы сегодня же проведём, посвящена исследованию, можно ли восстановить функцию сердца до исходных значений, применив фармакологический препарат, — поясняет Максим Жульков. — Мы определяем, что эта функция снижена, это естественное состояние, потому что дисфункция, развивающаяся после остановки кровообращения, прогрессирует, увеличивается с течением времени. Но у нас есть возможность скорректировать её и достичь дооперационного и пригодного к пересадке состояния миокарда.
По словам учёного, во всех 13 проведённых экспериментах удавалось достичь полного восстановления функции органа, который в итоге должен стать годным к трансплантации.
— То, что сердце после его остановки может быть оживлено даже спустя продолжительное время, мы воспринимаем как эффективный источник донорского органа, потому что в противном случае это сердце будет просто потеряно, — говорит Максим Жульков. — 20 минут — на самом деле это много. По данным зарубежных исследований, применение технологии оживления сердца после его остановки позволяет увеличить пул донорских органов на 20–30 процентов. Это способно покрыть тот лист ожидания, в котором находятся наши пациенты — реципиенты. Но даже за рубежом, к сожалению, эти технологии внедряются очень медленно. Это связано и с неоднозначными и нестандартизированными подходами к критериям оценки, к протоколу. В разных странах применяют разный временной промежуток между остановкой сердца и признанием его остановленным, после чего можно начать применять какие-то процедуры по оживлению и использованию для трансплантации. Это сложная тема, потому что внедрение в клинику разрабатываемых здесь подходов потребует решения огромного количества задач: юридических, организационных, технических, финансовых и морально-этических.
По результатам серии проводимых экспериментов разрабатывается протокол диагностического скрининга для оценки пригодности к трансплантации оживлённого органа. Он должен содержать рекомендации для клинического внедрения полученных в ходе эксперимента результатов.

Эксперименты учёных клиники подтверждают возможность вернуть функцию сердца к исходным значениям.
Продолжается и изучение фармакологических препаратов, которые могут быть эффективны при реанимации остановившегося донорского сердца. Их поиск и оценка эффективности — ещё одна часть исследования учёных.
Методика оживления сердца после его остановки — не единственная разработка группы. Другое не менее перспективное направление касается сохранения изъятого у донора сердца и его транспортировки на дальние расстояния.
По словам Максима Жулькова, в России основным способом сохранения органа остаётся фармакохолодовая консервация — сердце останавливается с помощью специального раствора, охлаждается и транспортируется при 4–6 градусах Цельсия. Но в таком случае функциональные способности органа стремительно ухудшаются с течением времени. В клинике же разрабатывают метод нормотермической аутоперфузии, то есть сохранения изъятых донорских органов, при котором они поддерживаются в рабочем состоянии вне тела с помощью перфузии собственной кровью или специальным раствором. Разработка специалистов клиники представляет собой небольшую транспортную мобильную систему, способную реанимировать орган, восстановить его функцию и провести динамическую оценку — проверить, может ли сердце перекачивать необходимый реципиенту объём крови. Эта система должна обладать способностью применяться при транспортировке на дальние расстояния, быть мобильной, автономной, поддерживающей температуру и обеспечивающей жизнедеятельность сердца изолированно от тела.
— За рубежом уже есть готовые транспортные системы, которые позволяют изъять орган пациента после смерти мозга и восстанавливать функцию изолированно, не используя подключение всего тела к кровообращению, — рассказал Максим Жульков. — У нас пока таких устройств нет. Но это не запрещает нам разрабатывать технологию и отвечать на вопросы, какое время остановки сердца безопасно, как восстанавливать его функцию, как понять, пригодно ли оно для пересадки. Визуально оно может продолжать сокращаться, но, будучи пересаженным, оказаться неспособным перекачивать нужный объём крови. Наша технология на основе аутоперфузии уникальна тем, что донорское сердце на всех этапах самостоятельно обеспечивает собственное кровоснабжение, работает в полную силу, а не сокращается «вхолостую».
Большинство технических решений, применяемых в разработках молодых учёных клиники, — авторские, защищённые патентами и отличные от тех, что используют в других странах. Работы проводятся на средства гранта Российского научного фонда и рассчитаны до 2027 года.

Материалы по теме:
Спасти сотни человеческих жизней поможет новая разработка новосибирских учёных — уникальный контейнер для сохранения донорского сердца
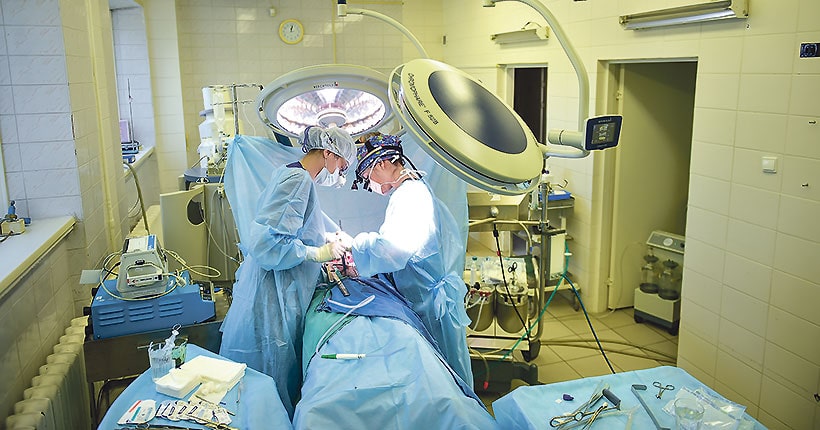
Усовершенствованные протезы для артерий и контейнеры для донорских сердец — какие разработки новосибирских учёных спасут жизни людей?

Один донор и четыре успешные операции по пересадке органов — в Новосибирской области активно развивается трансплантология

В Новосибирске побывал главный трансплантолог России. Региону поставлена задача увеличить количество пересадок органов в 10 раз

В Новосибирске заложили липовую аллею в знак благодарности тем, кто стал донором органов
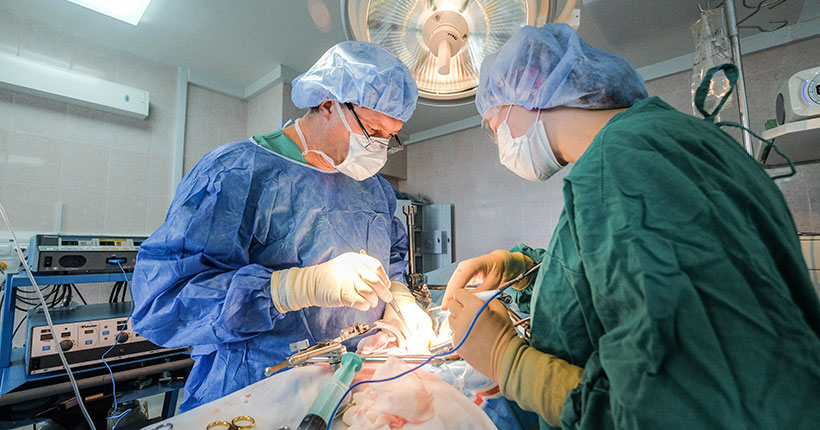
Существует ли «чёрный» рынок человеческих органов, где проводят операции по их пересадке и кто может стать донором?



